Apa itu EDTA ?
EDTA singkatan dari Ethylene Diamine Tetra Acetic acid
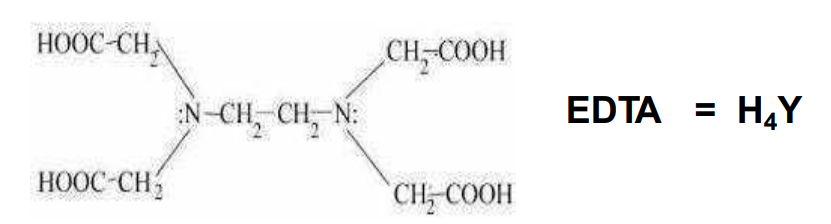
EDTA memiliki empat gugus karboksilat dan dua gugus amina
EDTA biasanya ditulis dalam bentuk asamnya dan singkat menjadi simbol H4Y
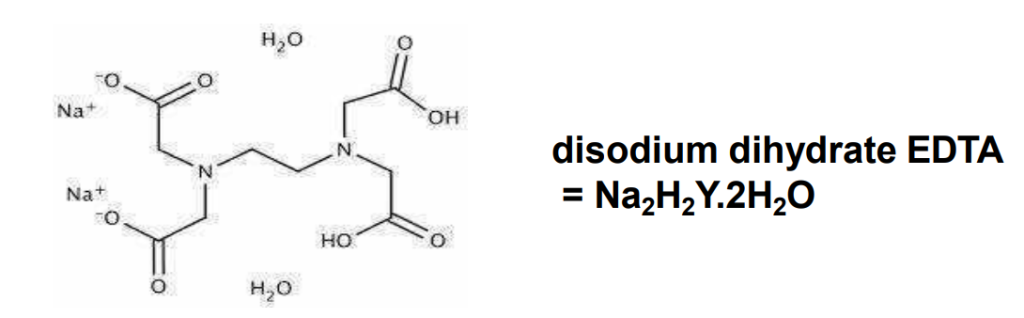
Disebbakan tingkat kelarutan EDTA yang rendah dalam air maka larutan standar EDTA dalam titrasi kompleksometri biasanya di buat dari garam natriumnya yaitu garam dinatrium EDTA dihidrat atau Na2H2Y.2H2O
Berbagai macam bentuk EDTA dalam lingkungan yang berbeda pHnya
EDTA dalam bentuk asam yaitu H4Y pada pH <3 Pada kisaran pH 3-10 maka spesies yang mendominasi adalah H2Y2- dan H3Y- Pada pH > 10 semua atom hidrogennya akan terprotonasi sehingga akan tinggal dalam bentuk Y4-
EDTA adalah ligan heksadentat dimana dia dapat menyumbangkan enam pasangan elektron bebasnya untuk membentuk ikatan kovalen koordinasi dengan kation untuk membentuk kompleks logam-EDTA

Aturan titrasi dengan menggunakan larutan standar EDTA
- Titrasi dengan menggunakan EDTA harus di lakukan dalam medium yang di buffer pada pH tertentu sesuai dengan kestabilan ion logamnya
- Penggunaan pH yang tepat sangat penting untuk konstanta kestabilan kompleks logam-EDTA
- Reaksi disosiasi asam dari EDTA, H4Y juga di pengaruhi oleh pH, dan pH ini juga berpengaruh untuk berfungsinya indikator
Mengapa larutan EDTA perlu di standarisasi?
- Larutan standar EDTA biasanya disiapkan dari garam natriumnya yang lebih mudah larut dalam air
- Tidak mudah menemukan garam natrium edta dalam keadaan yang murni
- Oleh karena itu larutan standar EDTA perlu dilakukan standarisasi
Bagaimana melakukan standarisasi larutan EDTA dengan menggunakan ZnO ?
- Larutan EDTA di standarisasi dengan menggunakan standar primer ZnO
- Titrasi dilakukan dengan menggunakan buffer pH 10 dan Eriochrome Black T sebagai indikator
- Titik akhir titrasi diamati dari perubahan warna dari ungu ke biru
Pembuatan larutan EDTA
- Timbang sekitar 3.8 g EDTA-2Na.2H2O dan larutkan dalam 300 mL aquades
- Encerkan dalam labu ukur hingga volumenya 1000 mL
- Simpan larutan ini dalam botol polietilen
Pembuatan larutan standar primer
- Timbang secara akurat 0.18 zat standar primer ZnO (panasakan dalam oven bersuhu 800 C hingga massanya tetap)
- Larutkan dalam 10 mL larutan HCl 4 M
- Encerkan hingga volumenya menjadi 250 mL
Prosedur standarisasi
- Pipet secara akurat 25 mL larutan EDTA dan tambahkan 1 tetes larutan 0,2% metil merah dalam etanol
- Tambahkan larutan amoniak hingga larutan berwarna kekuningan
- Tambahkan 25 aquades, 10 mL larutan buffer pH 10 dan 1-2 tetes indikator Eriochrome Black T
- Lakukan titrasi dengan larutan standar primer sampai terjadi perubahan warna dari unggu ke biru






