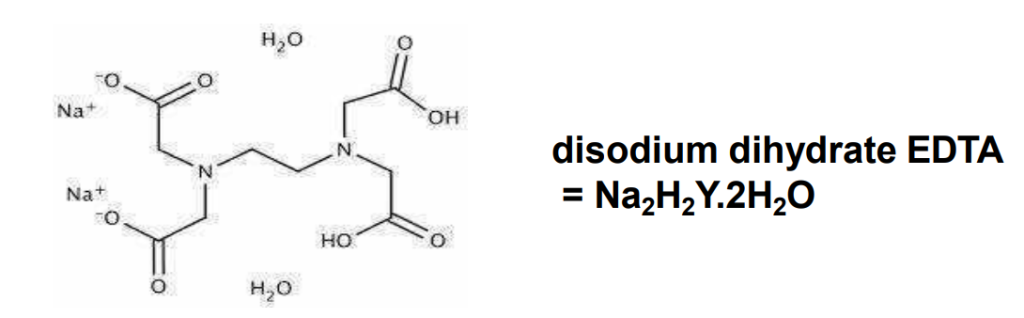
Metode visual yang dapat di gunakan untuk menentukan titik akhir titrasi pada titrasi kompleksometri hampir semuanya melibatkan pembentukan kompleks antara indikator dengan ion logam. Pada titrasi kompleksometri yang menggunakan EDTA sebagai titran maka pM (-log [ion logam]) mengalami kenaikan secara lambat sampai dengan dicapainya titik ekuivalen, dan pada saat semua ion logam telah membentuk kompleks dengan EDTA maka peningkatan secara tajam pada pM terjadi.
Indikator yang digunakan dalam titrasi kompleksometri akan berubah warna pada saat semua logam telah habis bereaksi dan membentuk senyawa kompleks dengan EDTA. Perubahan ini dihasilkan dari beralihnya warna kompleks-indikator dengan warna indikator dalam keadaan bebasnya seperti yang digambarkan dalam reaksi berikut,

Perlu diingat bahwa reaksi kedua akan terjadi jika kestabilan MgY2- lebih tinggi jika dibandingkan dengan kestabilan MgInd-.
Banyak sekali senyawa organik yang dapat membentuk senyawa kompleks dengan ion logam dan menghasilkan warna tertentu akan tetapi hanya sedikit dari senyawa organik ini cocok untuk dijadikan indikator visual. Hal-hal yang menjadi perhitungan suatu indikator dapat dijadikan menjadi indikator visual dalam titrasi kompleksometri adalah sebagai berikut,
- Dengan menambah sejumlah kecil indikator perubahan warna yang dihasilkan sudah cukup intens
- Warna kontrast antara kompleks logam-indikator dengan indikator harus mudah di amati
- Kompleks logam-indikator memiliki kestabilan untuk memastikan perubahan warna yang dapat diamati, namun kestabilannya harus lebih rendah dibandingkan dengan kompleks logam-EDTA
- Perubahan kesetimbangan dari kompleks logam-indikator menjadi kompleks logam-EDTA harus terjadi dengan cepat
- Reaksi perubahan warna indikator harus bersifat selektif
- Indikator harus sensitif terhadap ion logam sehingga perubahan warna dapat dengan cepat diamati saat mendekati titik ekuivalen
- Indikator harus stabil dalam medium yang digunakan dalam titrasi
- Indikator harus stabil dalam masa penyimpanan
- Syarat diatas harus terpenuhi pada pH yang akan dilakukan saat titrasi
- Dapat dengan mudah di peroleh secara komersil dan dengan kemurnian yang tinggi
Indikator yang dipakai untuk titrasi kompleksometri umumnya adalah pewarna organik yang di kenal dengan nama ‘indikator metalokromik’. Tabel dibawah ditampilkan indikator metalokromik beserta range pH serta kation apa saja yang dapat digunakan untuk titrasi dengan indikator tersebut. Warna kompleks logam-indikator dapat dilihat secara jelas oleh mata dikisaran konsentrasi indikator antara 10exp-6 s/d 10exp-7.

Eriochrome Black T
Eriochrome Black T adalah indikator metalokromik yang sering diperrgunakan dalam titrasi kompleksomteri untuk menentukan sejumlah kation. Struktur dari Eriochrome Black T diperlihatkan dalam gambar berikut ini,
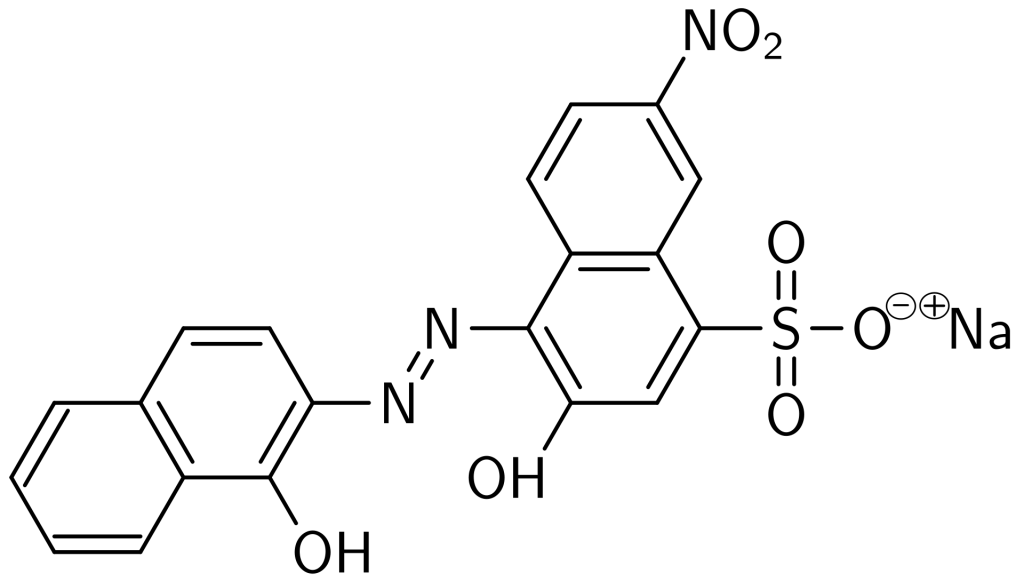
Eriochrome Black T bertindak sebagai asam lemah seperti reaksi berikut ini,

Ingat bahwa bentuk asam dan basa konjugasinya memiliki warna yang berbeda. Kompleks logam dengan Eriochrome Black T umumnya berwarna merah dimana dalam bentuk H2In-. Agar indikator berfungsi dengan baik maka pH larutan di set di nilai 7 ke atas agar bentuk bebas HIn2- mendominasi begitu ion logam semuanya habis bereaksi dengan EDTA dengan reaksi


tabung a berisi kompleks logam-indikator yang berwarna merah MIn- sedangkan gambar c adalah bentuk indikator bebasnya yaitu HIn2- sedangkan c adalah transisi warna dalam titrasi kompleksomteri menjadi warna ungu karena campuran antara warna merah dan biru dari a dan c