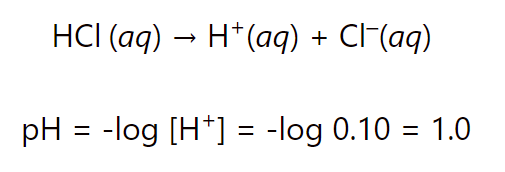Pembuatan kurva titrasi untuk basa kuat dan asam kuat dapat dilakukan dengan cara yang sama seperti saat kita membuat kurva titrasi asam kuat dengan basa kuat.
Cek disini cara membuat kurva titrasi asam kuat dengan basa kuat
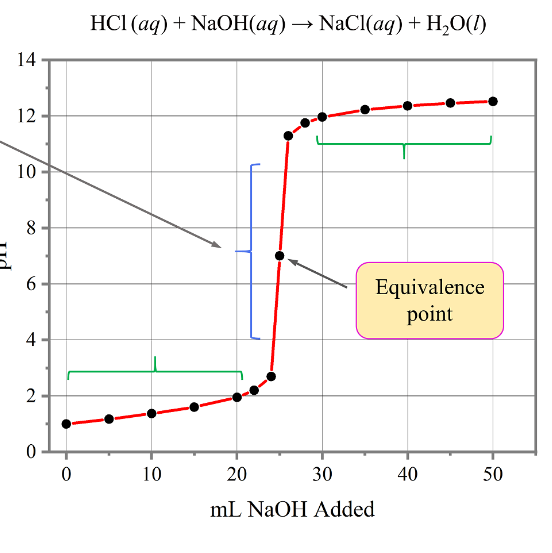
Sekarang marilah kita perhatikan contoh titrasi 0.1 M NaOH 25 mL dengan 0,1 M HCl.
pH saat penambahan 0 mL HCl
Didalam larutan hanya terdapat 0,1 M NaOH 25 mL maka kita harus mencari mol mula-mula NaOH dan kemudian mencari pH nya
pOH = – log [OH-] = – log [0,1] = 1
pH = 14 -1 = 13
pH saat penambahan 5 mL HCl
Pertama kit amenghitung mol HCl dan kemudian membuat perhitungan MBS (mulamula-bereaksii-sisa) untuk mencari berapa sisa NaOH yang terdapat didalam erlenmeyer dengan perhitungan sebagai berikut. Ingat sisa mol NaOH harus dibagi dengan volume total (vol NaOH + vol penambahan HCl)

Untuk penambahan 10 mL – 24,9 mL maka kita dapat menggunakan perhitungan yang sama seperti diatas ya. Yang perlu diperhatikan disini adalah bahwa semakin mendekati titik ekuivalen maka jumlah mol H+ akan mendekati jumlah mol OH-
pH penambahan 25 mL HCl
Saat penambahan 25 mL HCl maka mol asam adalah 2,5 mmol sedangkan mol basa NaOH juga 2,5 mmol. Artinya jumlah mol asam sama dengan jumlah mol basa dan karena perbandingan mol reaksi antara NaOH dan HCl adalah 1:1 maka baik HCl dan NaOH akan habis bereaksi sehingga yang tertinggal sekarang adalah garam NaCl.
NaCl adalah garam yang terbuat dari asam kuat dan basa kuat dalam larutan tidak terhidrolisis sehingga pH nya adalah 7.
pH setelah penambahan 30 mL HCl
Setelah penambahan 30 mL HCl maka mol asam klorida adalah 3,0 mmol sedangkan mol basa 2,5 mmol, ini artinya saat ini ada kelebihan basa sebesar 0,5 mmol, dan pH nya dapat dicari dengan menggunakan rumus

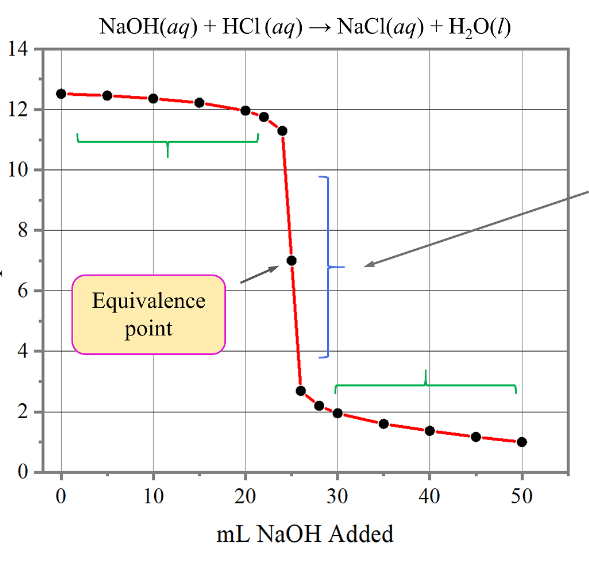
Untuk menghitung pH penambahan HCl dari 35 mL sampai 50 mL kita bisa menggunakan perhitungan yang sama seperti diatas ya . Dan jika di plot kurvanya akan tampak seperti gambar berikut ini,