Hitunglah konsentrasi molar analitik dan konsentrasi molar kesetimbangan larutan di dalam air yang dibuat dari 285 mg asam trikloroasetat Cl3CCOOH (mr = 163.4 g/mol) dalam 10 mL air (asam ini terionisasi 73% dalam larutan )


Hitunglah konsentrasi molar analitik dan konsentrasi molar kesetimbangan larutan di dalam air yang dibuat dari 285 mg asam trikloroasetat Cl3CCOOH (mr = 163.4 g/mol) dalam 10 mL air (asam ini terionisasi 73% dalam larutan )


Berapakah molaritas ion K+ dalam suatu larutan yang mengandung 63.3 ppm K3Fe(CN)6 (mr = 329.3 g/mol)
Jawab:
tips mengerjakan soal seperti ini


Hitunglah konsentrasi molar larutan HNO3 (Mr=63.0 g/mol) yang memiliki spesifik graviti 1.42 dan 70.5% w/w HCl
Jawab:
Untuk menjawab soal ini maka kita perlu mengubah satuan HCl pekat diatas menjadi satuan g/L HCl, selanjutnya dengan membagi dengan Mr HCl kita memperoleh molaritas HCl pekat


Diskripsikan pembuatan 6 M HCl 100 mL yang di buat dari larutan HCl pekat yang memiliki spesifik graviti 1.18 dan 37% w/w HCl (Mr HCl = 36.5 g/mol)
Jawab:
Untuk menjawab soal ini kita pertama harus menghitung berapa M larutan HCl pekat yang memiliki spesifik graviti 1.18 dan 37% w/w HCl setelah itu dengan menggunakan rumus pengencaran kit adapat mengetahui berapa mL HCl pekat yang dibutuhkan


Bagaimana cara membuat larutan 0.0740 M Cl- yang dibuat dari BaCl2.2H2O ?
Jawab:
Cara mengerjakan soal ini adalah dengan mengkonversi mol ion Cl- ke dalam mol BaCl2.2H2O selanjutnya dari sini kit amengkalikan dengan mr BaCl2.2H2O untuk mendapatkan massanya .


Kimiawan kimia analisa seringkali mengekspresikan konsentrasi dalam satuan persen (bagian per seratus). Sayangnya dalam prakteknya hal ini sering mengalami ambigu disebabkan komposisi dalam prosentase dapat dinyatakan dalam berbagai varibel contohnya
Dan cara menghitung ketiga besaran diatas adalah sebagai berikut,

Perlu diingat bahwa penyebut dari perhitungan diatas adlah selalu larutan bukan pelarutnya. Perlu diingat juga bahwa unit untuk dua persamaan pertama tidak perlu disebutkan sedangkan untuk persamaan ketiga harus disebutkan karena unit antara pembilang dan penyebutnya tidak sama.
prosentase berat biasanya dipakai untuk mengekspresikan konsentrasi larutan komersial contohnya asam nitrat pekat dijual dengan prosentase berat 70% yang artinya terdapat 70 g HNO3 dalam 100 g larutan. Prosentase volume biasanya dipakai untuk mengekspresikan konsentrasi larutan yang dibuatdari cairan murni yang di encerkan ke dalam pelarut. Contohnya 5% volume etanol artinya terdapat 5 mL etanol yang diencerkan dalam 95 mL air.
Prosentase berat per volume biasa dipakai untuk merujuk pada reagen padat yang di larutkan dalam air. Contoh larutan 5% w/v perak nitrat artinya terdapat 5 g AgNO3 yang dilarutkan dalam air sehingga volumenya menjadi 100 mL.
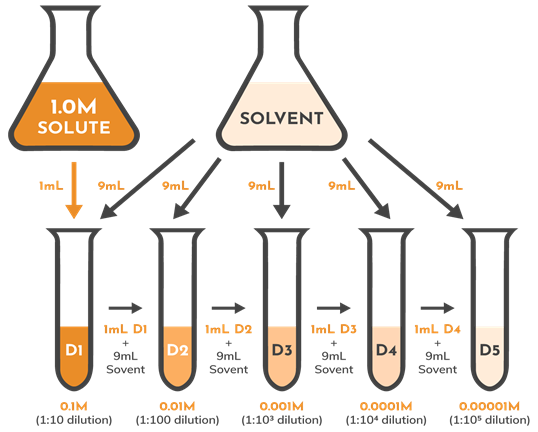
Apa itu rasio pengenceran ?
Rasio pengenceran adalah rasio zat terlarut (zat yang akan diencerkan) dengan pelarut (contoh air). Sebagai contoh jika kita punya rasio pengenceran 1:3 maka artinya kita menambahkan 1 unit volume zat terlarut (zat yang akan diencerkan) dengan 3 unit volume pelarut contohnya air dimana akan menghasilkan 4 unit total volume.
Mengapa rasio pengenceran sangat penting? dalam kehidupan sehari-hari biasanya kita menemukan produk pembersih yang harus diencerkan sebelum di pergunakan. Nah dengan mengetahui bagaimana rasio pengenceran ini maka kita akan dapat menggunakan produk komersial itu dengan benar.
Contoh soal rasio pengenceran
Kamu punya wadah dengan volume 1 liter, nah kamu ingin mengencerkan pembersih kamar mandi dimana pada label botolnya tertulis rasio antara air dengan pembersih seharusnya 3:1 (3 bagian air dan 1 bagian pembersih)
Pertama kita hitung dulu volume pembersih
= volume final / (rasio pelarut + rasio zat terlarut)
= 1 liter / (3+1)
= 0,25 liter
Nah ini artinya kita harus mencampurkan 0,25 liter zat pembersih dengan 0,75 liter air untuk menghasilkan 1 liter larutan pembersih.
Apa yang dimaksud dengan Faktor pengenceran ?
Jika rasio pengenceran menginformasikan kepada kita perbandingan antara zat terlarut dengan zat pelarut. Sebagai contoh rasio pengenceran 1:4 maka artinya anda mencampur 1 unit zat yang akan diencerkan dengan 4 unit pelarut untuk menghasilkan total 5 unit volume.
Sedangkan faktor pengenceran adalah menyatakan perbandingan antara zat terlarut (zat yang akan diencerkan dengan volume total larutan yang dihasilkan. Contoh faktor pengenceran 1:4 artinya anda mencampurkan 1 unit volume zat yang akan diencerkan dengan 3 unit volume pelarut untuk menghasilkan total volume 4.

Ilmuwan sering kali mengekspresikan konsentrasi spesies dalam bentuk fungsi-p atau p-value atau nilai-p. Salah satu contohnya adalah pH. Di dalam tulisan pH, huruf ‘p’ mengindikasikan ‘potensial’ atau kita dapat mengatakan ‘power’. Jadi pH berarti potensial hidrogen atau power hidrogen.
Nilai-p juga dapat diartikan sebagai logaritma negatif dari suatu spesies. Jika ingin menjadi nilai p dari suatu konsentrasi X maka kita dapat mendefinisikannya sebagai berikut

Mengekspresikan nilai suatu spesies dalam bentuk nilai-p memiliki salah satu manfaat yakni alih-alih menggunakan bilangan persepuluan atau bilangan berpangkat sepuluh maka kita dapat menyatakan konsentrasi suatu spesies hanya dengan bilangan positif yang keci.
Contoh:
Nyatakan konsentrasi H+ dalam HCl 0,00054 M dalam bentuk nilai-p
pH = – loh [H+] = – log [0,00054] = 3,27

Untuk menyatakan konsentrasi larutan yang sangat encer kita dapat menyatakannya dengan menggunakan ppm atau bagian persejuta dan ppb atau bagaian per miliar. Dimana untuk ppm maka di definisikan sebagai berikut,

sedangkan untuk ppb maka dirumuskan sebagai berikut,

Untuk larutan yang sangat encer dimana densitas larutan bisa dianggap 1 g/mL maka 1 ppm = 1 mg /L larutan . Sedangkan untuk ppb maka 1 ppb = 1 ug/L (mikrogram per liter )
Contoh 1 :
Berapakah ppm jika terdapat 2 mg ion Ca2+ dalam setiap 1 liter air sungai ?

Contoh :
Berapakah molaritas ion K+ yang berisi 63,3 ppm K3Fe(CN)6 (329 g/mol) ?


Densitas dan Specific Gravity adalah istilaha umum yang banyak di temui dalam literatur kimia analisis. Keduanya memiliki pengertian yang berbeda, jangan sampai salah yang memaknai kedua istilah tersebut.
Densitas
Dinyatakan dalam bentuk pembagian antara massa larutan dengan volume larutan. Dalam satuan internasional (SI) densitas memiliki satuan Kg/m3 atau g/mL
Densitas = Massa larutan / Volume larutan
Specific Gravity
Specific Gravity disebut juga dengan densitas relatif. Specific gravity di definisikan sebagai perbandingan densitas suatu zat dengan zat referensi. Untuk specific gravity cairan maka dibandingkan dengan densitas air pada suhu 4 derajat celcius. Sedangkan specific gravity untuk gas maka dibandingan dengan densitas udara pada suhu ruang yaitu 20 derajat celcius.
rumus specific gravity atau densitas relatif

sedangkan untuk mencari densitas zat tersebut dihitung sebgaai berikut
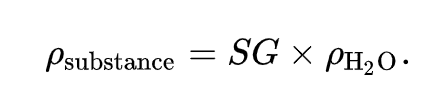
Densitas air pada suhu 4 derajat celcius adalah 1000 kg/m3 atau 1 g/mL, dengan alasan inilah maka kadangkala specific gravity dengan densitas sering dianggap sama.
Specific gravity tidak memiliki satuan dan sering dipergunakan dalam istilah komersial. Jika specific gravity zat tersebut nilainya lebih besar dari 1 maka cairan tersebut akan tenggelam di dalam air. Jika densitas relatifnya sama dengan 1 maka maka volume zat yang sama keduanya memiliki massa yang sama dan zat terebut akan melayang di dalam air. Namun jika zat tersebut memiliki specific gravity kurang dari 1 maka zat tersebut akan terapung dalam air. Contoh es memiliki specific gravity 0,91 maka es akan terapung jika dimasukan dalam air.
Nilai specific gravity beberapa larutan asam komersial adalah sebagai berikut,
