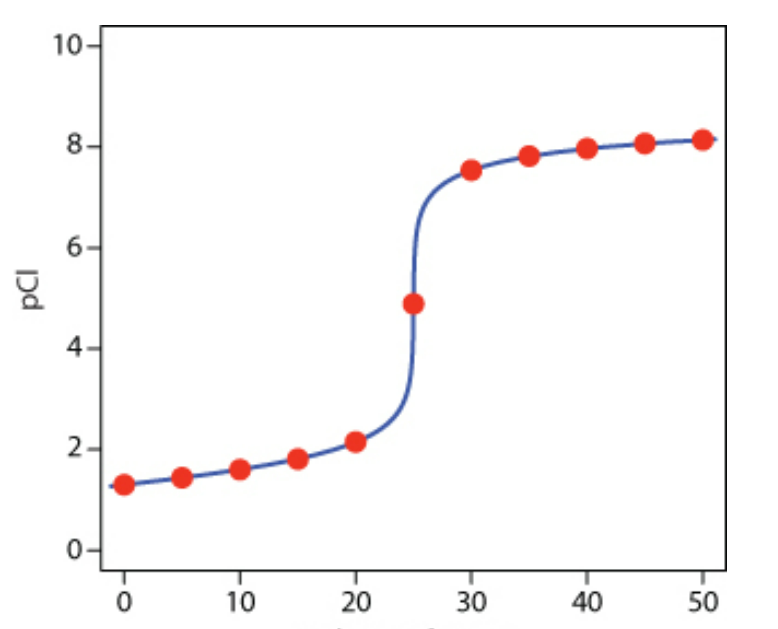
Kurva titrasi Argentometri dapat dibuat dengan cara memplot antara pCl analit dengan volume larutan baku AgNO3 (contoh gambar diatas). Misalkan kita punya analit 50 mL NaCl 0.05 M yang akan ditritasi dengan larutan AgNO3 0,1 M.
Pertama yang kita lakukan adalah menghitung pCl larutan NaCl sebelum larutan baku AgNO3 ditambahkan.
[Cl-] = 0.05 M
pCl = -log [Cl-] = – log (0.05) = 1.30
Setelah itu setelah penambahan 5 mL AgNO3 0.1 M maka,
konsentrasi [Cl-] sisa
= mol Cl- awal – mol Ag+
= (0,05 x 50) – (5 x 0.1)
= 2,5 – 0,5
= 2 mmol
Konsentrasi Cl-
= mol Cl- / ( volume NaCl + Vol Ag NO3)
= 2 mmol / (50+5)
= 0,0363
pCl
= -log [Cl-]
= – log (0.0363)
= 1,44
Dengan menggunakan cara yang sama untuk setiap penambahan 5 mL AgNo3 maka kita akan mendapatkan data seperti berikut,

Note
Untuk perhitungan setelah titik ekuivalen terjadi maka kita dapat menghitung konsentrasi Cl- dengan menggunakan harga Ksp dimana konsentrasi Ag+ yang berlebih kita masukan ke dalam rumus Ksp guna mendapatkan konsentrasi Cl- seperti contoh perhitungan berikut setelah penambahan 35 mL AgNO

Dengan mengeplot nilai pCl dengan volume AgNO3 maka gambar kurva yang kita peroleh adalah seperti gambar kurva diatas.
Leave a Reply