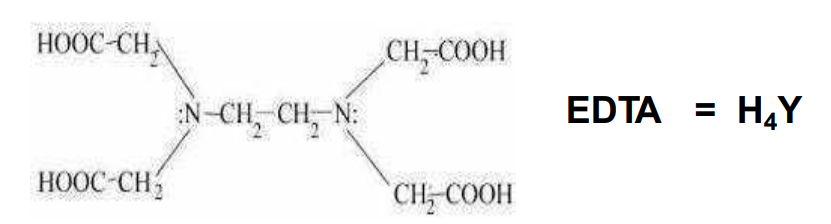
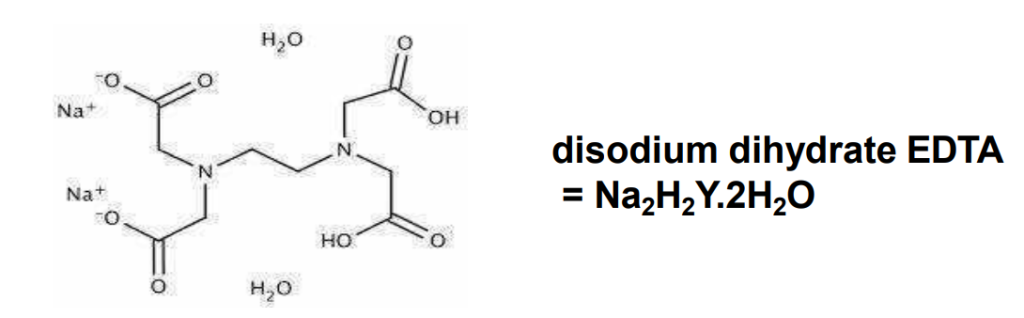
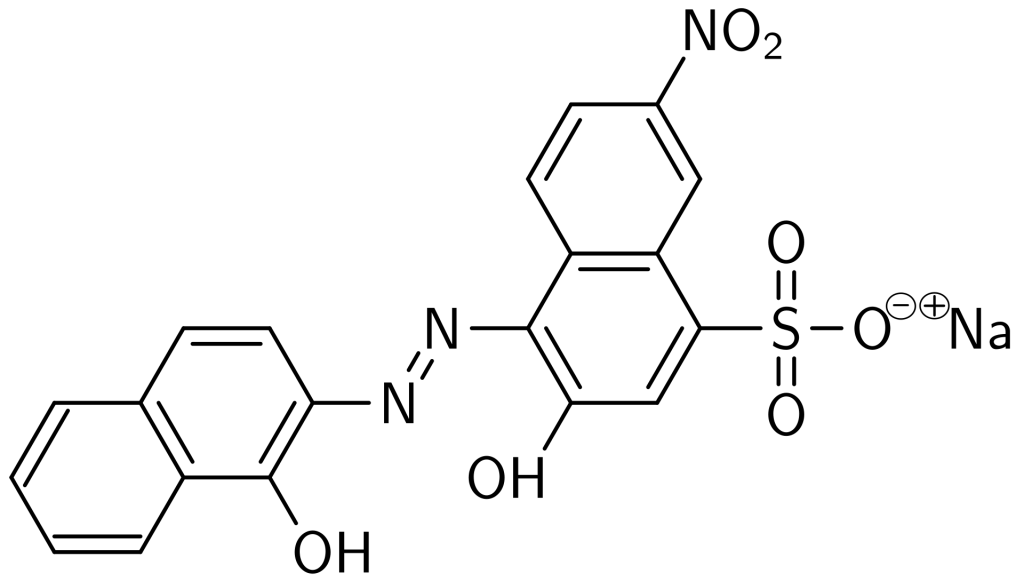
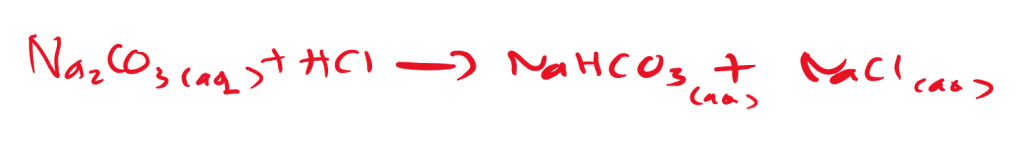Terdapat lima jenis teknik titrasi kompleksometri dengan menggunakan larutan standar EDTA yaitu,
- Titrasi langsung
- Titrasi kembali
- Titrasi substitusi
- Titrasi alkalimetri
- Titrasi tidak langsung
Titrasi langsung
- Titrasi ini dilakukan dengan mentitrasi secara langsung larutan ion logam dengan menggunakan larutan standar EDTA
- Larutan analit berisi ion logam yang di buffer dengan pH tertentu dan selanjutnya di titrasi dengan EDTA
- Zat tambahan seperti tartarat dapat ditambahkan untuk mencegah timbulnya endapan hidroksida dari ion logam
- Kation yang dapat di titrasi dengan metode langsung ini adalah Cu2+, Zn2+, dan Ni2+
Titrasi Kembali
- Metode ini menggunakan larutan standar EDTA berlebih yang ditambahkan ke dalam larutan ion logam
- Larutan akan terdapat EDTA yang tidak bereaksi yang kemudian bisa dititrasi dengan menggunakan larutan standar ion logam dengan adanya indikator. Larutan ZnCl2, ZnSO4, MgCl2, dan MgSO4 dapat di pakai sebagai larutan standar ion logam
- Kation yang dapat dilakukan titrasi dengan metode ini adalah Al3+, Co2+, Pb2+, Mn2+, Hg2+, dan Ni2+
Titrasi Substitusi
- Metode ini menggunakan kompleks logam-EDTA yang lebih lemah misalnya ion logam M2 yang ditambahkan ke dalam larutan ion logam M1 yang akan ditentukan kandungannya.
- Mg-EDTA atau Zn-EDTA biasanya di pakai sebagai kompleks logam kedua yang lebih lemah
- Kompleks logam-EDTA yang lebih lemah nantinya akan digantikan dengan kompleks logam yang lebih kuat
- Jumlah ekuivalen logam M2 yang dibebaskan dapat dititrasi dengan larutan stdandar EDTA
- Metode ini biasanya dapat dipergunakan untuk menentukan kation Ca2+
Titrasi Alkalimetri
- Metode ini menggunakan prinsip bahwa reaksi EDTA H2Y2- dengan ion logam akan membebaskan ion H+
- Ion H+ yang di bebaskan ini dapat di titrasi dengan larutan alkali contohnya NaOH dengan menggunakan indikator yang sesuai
Titrasi Tidak Langsung
- Metode ini dipakai untuk menentukan ion halida, fosfat atau sulfat yang mana tidak membentuk kompleks dengan EDTA
- Untuk menentukan SO42- misalnya maka larutan di tambahkan dengan larutan standar barium dalam keadaan berlebih
- Endapat BaSO4 kemudian di filtrasi dan ion barium yang tidak bereaksi dengan SO42- dapat di titrasi dengan EDTA
- Dengan cara ini maka secara tidak langsung kita dapat menentukan jumlah ion sulfat dalam analit.