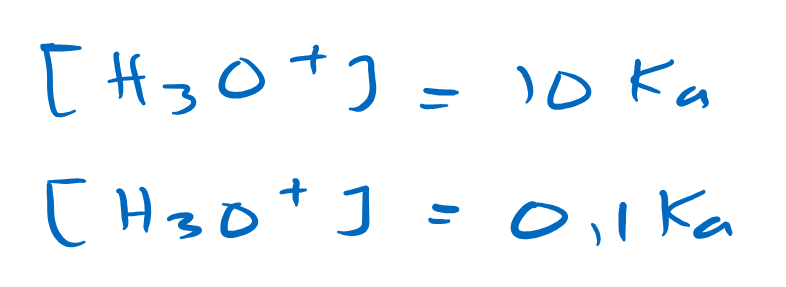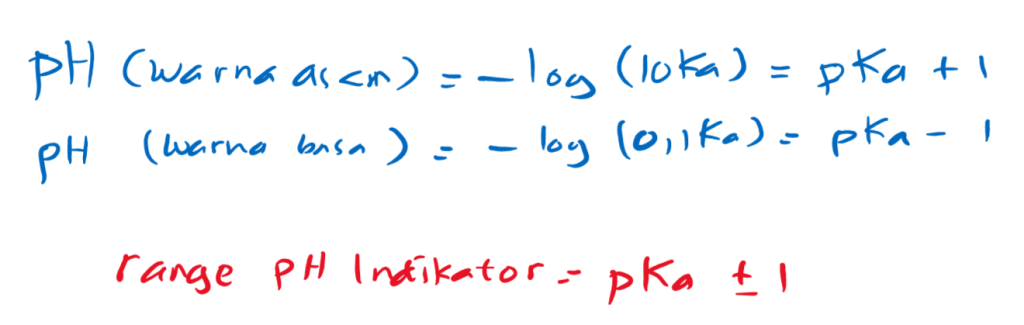Terdapat dua jenis titrasi eror pada titrasi asam basa yang berhubungan dengan indikator. Titrasi eror pertama terjadi pada saat kesalahan menentukan perbedaan pH antara pH pada saat indikator berubah warna dengan pH titik ekuivalen. Apabila terjadi hal yang demikian maka solusinya adalah dengan cara memilih jenis indikator yang nantinya akan dipergunakan dalam titrasi atau dengan membuat koreksi dengan titrasi blanko.
Jenis titrasi eror yang kedua adalah berasal dari keterbatasan penghilatan mata orang yang melakukan titrasi untuk mengamati perubahan warna walau perubahannya sangat kecil. Hal ini tentu saja akan mempengaruhi kualitas pengulangan titrasi yang akan dilakukan. Bisa saja warna pengyulangan titrasi yang kedua dan seterusnya memiliki perbedaan warna pada titrasi yang pertama.
Besarnya kesalahan yang menyebabkan hal tersebut terjadi dipengaruhi oleh perubahan pH permililiter reagent pada saat terjadinya titik ekuivalen, konsentrasi indikator, dan sensitifitas mata pengamat saat terjadinya perubahan warna indikator.
Rata-rata ketidakpastian visual saat kita menggunakan indikator pada titrasi asam basa adalah antara +-0,5 s/d +-1 unit pH. Ketidakpastian ini dapat diperkecil hingga -+0,1 unit pH dengan cara mencocokan warna larutan yang telah dititrasi dengan larutan yang berisi sejumlah indikator yang sama pada pH tertentu.
Variabel yang menentukan perubahan sifat indikator
Interval pH pada saat indikator mengalami perubahan warna dipengaruhi oleh temperatur, kekuatan ion dari spesies yang terdapat di dalam larutan, adanya kehadiran pelarut organik, dan adanya partikel koloid. Dua yang disebutkan terakhir dapat menyebabkan pergeseran pH perubahan warna indikator sampai dengan 1 atau lebih unit pH.
Indikator Umum Yang di pergunakan pada titrasi asam basa
Daftar di bawah ini adalah beberapa indikator yang biasa dipergunakan untuk titrasi asam basa, beserta range pH indikator masing-masing. Perlu diperhatikan bahwa range pH indikator dibawah ini berkisar antara 1,1-2.2 dengan rata-rata 1,6 .